VACUNA
27 de julio de 2021
Ultra pediátrica: cómo será la vacuna contra el COVID que investiga Pfizer en niños
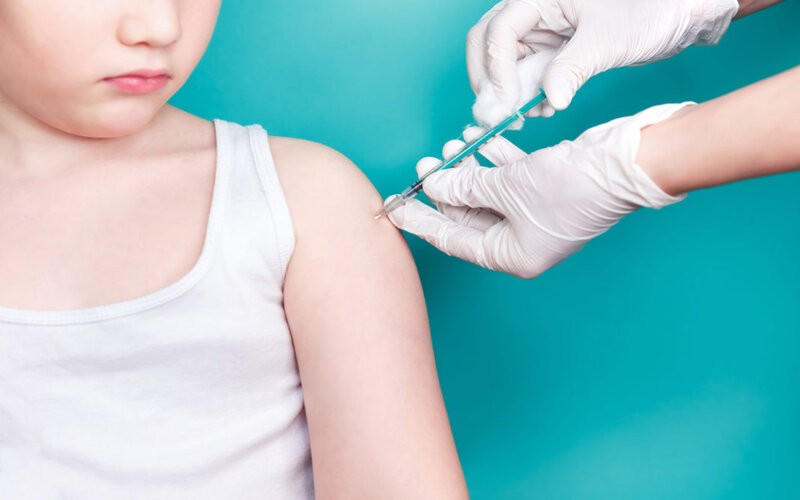
Antes de fin de año el laboratorio Pfizer a ultima un ensayo clínico de Fase II / III para disponer de una vacuna contra el COVID-19 de plataforma genética (ARN mensajero) para niños desde 11 años hasta bebés de 6 meses
Infobae entrevistó al científico Rodrigo Sini de Almeida, líder del ensayo clínico global de Fase II/III de Pfizer, sobre vacunas contra el COVID-19 para pediátricos. Participan varios países del mundo y quedó afuera la Argentina. Serán inoculaciones que estarán disponibles de manera escalonada por rangos etarios entre finales de 2021 y comienzos de 2022. Existe consenso entre los expertos que allí radica el comienzo del final de la pandemia
Llegó el tiempo de vacunar a los niños contra el COVID-19 mientras la pandemia global por coronavirus está cerca de cumplir 2 años, y aún circula robustecida alrededor del globo a través de las nuevas variantes o “trajes” que tan eficazmente aprendió a usar el virus SARS-COV-2, para perdurar en el tiempo entre sus huéspedes favoritos, los seres humanos.
La necesidad de incluir a los adolescentes y niños para que sean vacunados contra el COVID-19 se vio reforzada por la vulnerabilidad en la que han quedado los más pequeños que padecen comorbilidades y porque la inmunización de los menores de edad, tanto sanos como enfermos, permitiría, según los expertos, frenar la ola de contagios que creció exponencialmente sobre todo, en la actualidad, en los países donde la variante Delta es de circulación comunitaria.
Hasta ahora el laboratorio Pfizer lidera la carrera de las vacunas pediátricas contra el COVID-19, seguido de cerca por Moderna y compartiendo la misma plataforma genética. La vacuna de Pfizer demostró ser 100% eficaz en la prevención del COVID-19 en adolescentes. Es la única -hasta el momento en el mundo -que recibió la autorización de emergencia de las dos reguladoras más importantes, -la norteamericana, FDA y la europea, EMA- para ser aplicada en menores desde los 17 hasta los 12 años, porque finalizó sus ensayos clínicos . Y ahora apuesta a “bajar” la edad con nuevos ensayos clínicos, en busca de evidencia y seguridad en adolescentes, niños y bebés.
En diálogo exclusivo con Infobae, Rodrigo Sini de Almeida, desde San Pablo, Brasil, director de asuntos médicos de vacunas para América Latina de Pfizer adelantó que entre fines de 2021 y comienzos de 2022 estará disponible la “vacuna ultra pediátrica” de Pfizer- de plataforma ARN mensajero- desde los 11 años hasta los 6 meses de vida.
Sini de Almeida explicó: "Estamos realizando la Fase II/III de este ensayo clínico en varios países del mundo. La investigación incluye a más de 4.600 participantes/voluntarios de diferentes partes del mundo que fueron divididos en tres grupos de edad: niños de 5 a 11 años, de 2 a 5 años y bebés de 6 meses a 2 años. Tenemos participantes niños y adolescentes de Estados Unidos, Finlandia, España y Polonia. Son más de 90 centros de estudios que fueron elegidos especialmente de acuerdo con su capacitación de recibir y seguir a esos niños. Tenemos una participación muy heterogénea y bien distribuida en el mapa".
"Este estudio que estamos haciendo actualmente FASE II/III para aplicar la vacuna COVID-19 en pediátricos tendrá entonces dos grandes etapas etarias: primero, de 11 a 5 años y luego una segunda etapa, desde los 12 años hasta los 6 meses de vida. El arco completo de vacunas contra el COVID-19 aptas para niños de 11 años hasta los 6 meses de vida estarían listas para ser aplicadas a comienzos de 2022", añadió.
El objetivo es que este año América Latina pueda disponer de una vacuna pediátrica contra el COVID-19, con la misma tecnología que se creó para la vacuna de los adultos, la plataforma producida por ingeniería genética-sintética de ARN mensajero. La investigación en adolescentes y niños se lleva adelante de forma escalonada, desde los 11 años hasta los 6 meses de vida .
El ensayo clínico que lidera el doctor Sini de Almeida no contará con voluntarios en la Argentina; como sí ocurrió con el estudio de la vacuna Pfizer-Biontech para adultos en el 2020, en el Hospital Militar de CABA, considerado, el más grande del mundo. Lo lideró el infectólogo Fernando Polack, quien firmó y encabezó luego en la revista The New England Journal of Medicine el paper sobre eficacia y seguridad de la vacuna más innovadora y oportuna contra el COVID-19.
“Este ensayo clínico en pediátricos - adolescentes y niños- al trabajarlo de manera escalonada por segmentos etarios- tiene un proceso innovador, de trabajo conjunto en diferentes frentes. Tenemos la expectativa para octubre 2021 de tener los resultados del segmento 5 a 11 años; y a finales de este año contar con las aprobaciones bajo uso de emergencia. Los datos de los niños de 2 a 5 años podrían llegar poco después y en los de 6 meses a 2 años estimó que reuniría los informes necesarios hacia octubre o noviembre para presentarlos ante la FDA. Una vez que superemos los diferentes procesos que establecen los órganos regulatorios, esperamos cuanto antes seguir con este proceso de vanguardia de resultados”, agregó Sini de Almeida. (N. de la R.: ayer la FDA pidió que Pfizer y Moderna amplíen el estudio de sus vacunas en niños de 5 a 11 años y que agreguen 3.000 niños en ese grupo de edad. Se trata de una medida de precaución diseñada para detectar efectos secundarios raros).
Sini de Almeida es brasileño e investigador líder en el área vacunas de Pfizer. Vive actualmente en San Pablo. Y es médico pediatra especializado en enfermedades infecciosas pediátricas y miembro de la Sociedad Brasileña de Pediatría y de la Sociedad Europea de Enfermedades Infecciosas Pediátricas.
Consultado sobre cómo equilibrar en el caso de la vacunación pediátrica dos ideas que muchas veces colisionan, y como ya ocurre con otras vacunas -por ejemplo con la vacuna del HPV- la tensión entre la tolerabilidad, la reactogenicidad y completar las dosis.
Sini de Almeida contestó: "Estos son temas muy importantes cuando se diseñan esquemas de vacunación pediátrica. Siempre debemos priorizar la seguridad y la eficacia. Es cierto que cuando hablamos de niños, hablamos de un calendario de muchas más vacunas, que en otras etapas de la vida. En el caso del COVID-19, todavía no tenemos estudios de co-administración. Como sí existe en otros tipos de vacunas, todavía trabajamos para entender la respuesta de la vacuna frente a la enfermedad en los diferentes rangos de edad".
"En este momento necesitamos la respuesta de las vacunas para los niños en general, para después buscar la complementariedad. En adultos, por ejemplo, ya empezamos a hacer estudios de co-administración con la vacuna de influenza, con la vacuna neumocócica conjugada de Pfizer- Biontech con la de COVID-19 para ver qué ocurre. Sería deseable que mientras la pandemia cede, podamos más adelante aplicar por ejemplo las vacunas de la influenza o neumocócica conjugada junto con la del COVID-19", manifestó.
En cuanto a cuáles son los aspectos más específicos entre una vacuna contra el COVID creada para niños y la versión para adultos. Tolerabilidad, posología, cantidad de dosis. Precisó: "¡Todo eso junto! Siempre cuando hablamos de ensayos clínicos de vacunas empezamos los estudios en adultos, y después bajamos las edades. Y claro que hay algunas características específicas en los niños y adolescentes. Hay que entender primero esos mecanismos intrínsecos. Por ejemplo, la respuesta inmune natural de un niño de 6, 7, 8 meses, es diferente a la de un niño de 5 años".
Y agregó: "Una cosa que observamos en los estudios clínicos es que en el segmento de 12 hasta 15 años, hay más reactogenicidad en esta población. Tienen mucho más dolor de cabeza, por ejemplo. Y cuando miramos a los mayores, la tolerabilidad es un punto muy importante. En todos los casos lo que siempre hay que evaluar es la seguridad. Hoy ya sabemos que la misma dosis que utilizamos de adultos (30mg) no será la misma en niños. Vamos a dar dosis mucho más bajas, pensando por ahora en dos dosis. ¿Por qué? Porque en ese rango de edad la vacuna genera una gran respuesta inmunogénica, y al mismo tiempo tiene mucha reactogenicidad, entonces necesitan menos cantidad de los principios activos de la fórmula original".
#Escuchá La 97.1 todo el día, hacé clickacá📻
#Descarga la App de #RTuc haciendo clickacá📲











Seguinos
+543816909015